- 国务院:三级综合医院应具备独立开展新冠病毒检测能力
- 科技部:批准建设国家人类疾病动物模型资源库
- 国家市场监督管理总局:口罩等防疫用品出口欧盟准入信息指南
- 国家药监局:2020年3月批准注册医疗器械产品目录
《核酸检测行业创新报告》
Lone Operator: How to Survive & Thrive in the Modern Age

哈哈
The first story
白
1
国务院:三级综合医院应具备独立开展新冠病毒检测能力
近日,国务院应对新型冠状病毒肺炎疫情联防联控机制综合组印发《关于进一步做好疫情期间新冠病毒检测有关工作的通知》,要求三级综合医院均应当建立符合生物安全二级及以上标准的临床检验实验室,具备独立开展新型冠状病毒检测的能力;各级疾控机构和有条件的专科医院、二级医院、独立设置的医学检验实验室也应当加强实验室建设,提高检测能力。
关于进一步做好疫情期间新冠病毒检测有关工作的通知
联防联控机制综发〔2020〕152号
各省、自治区、直辖市及新疆生产建设兵团卫生健康委:
新冠肺炎疫情发生以来,全国医疗机构和疾控机构迅速落实国家有关要求开展新冠病毒核酸检测工作,在疫情防控中发挥了重要作用。当前,复工复产逐步推进、疫情境外输入压力不断增大、离汉离鄂通道管控措施解除,以及无症状感染者存在一定传播风险等情况,对新冠病毒检测工作提出了新的要求。部分地区出现了实验室检测能力不足等问题,无法完全适应疫情防控需求。为进一步做好疫情期间新冠病毒检测工作,现将有关要求通知如下:
一、进一步加强实验室建设,提高检测能力
各地要结合新冠疫情防控和检测需求,加强医疗卫生机构实验室建设。三级综合医院均应当建立符合生物安全二级及以上标准的临床检验实验室,具备独立开展新型冠状病毒检测的能力;各级疾控机构和有条件的专科医院、二级医院、独立设置的医学检验实验室也应当加强实验室建设,提高检测能力。对医疗资源相对缺乏、检测能力相对薄弱、疫情防控压力较大的地区,特别是陆路边境口岸,要选择1家综合实力强的县级医疗机构予以重点支持,实现县域内医疗机构具备核酸检测能力。
二、落实实验室备案或准入要求,依法依规检测
新冠病毒检测应当由符合条件的医疗机构(包括独立设置的医学检验实验室)和疾控机构开展。医疗机构开展病原学检测应当具备在设区的市级人民政府卫生健康主管部门备案的生物安全二级及以上实验室资质,且符合《医疗机构临床基因扩增检验实验室管理办法》(卫办医政发〔2010〕194号)的要求,具有PCR实验室条件。医学检验实验室应当符合《医学检验实验室基本标准(试行)》和《医学检验实验室管理规范(试行)》(国卫医发〔2016〕37号)要求;医疗机构或疾控机构将新冠病毒检测业务委托给医学检验实验室开展的,应当按照要求与其签订相应协议,明确双方的权利义务。
三、加大医疗卫生人员培训力度,规范技术操作
各地要按照《新型冠状病毒肺炎实验室检测技术指南》(国卫办疾控函〔2020〕156号)要求,加强对医疗卫生人员的技术培训和指导,覆盖所有开展新冠病毒检测的医疗卫生机构,提高人员操作的规范性。要确保相关医务人员熟练掌握鼻咽拭子、咽拭子、下呼吸道标本、血液或血清标本、便标本的规范采集方法,实验室检测人员熟练掌握标本处理、相关试剂使用和检测方法,减少技术操作问题对检测结果准确性、可靠性的影响。实验室检测人员要经过严格的规范化培训,开展检测时做好生物安全防护。
四、加强实验室检测质量控制,提高检测质量
各实验室应当使用经药监部门批准的检测试剂和采样拭子,加强实验室室内质控,常态化接受国家级或省级临床检验质量控制。各省级卫生健康行政部门要组织辖区内开展新冠病毒检测的医疗机构分批参加室间质评,保证每家机构至少参加1次室间质评并合格。室间质评结果不合格的,不允许开展新冠病毒检测。国家卫生健康委临床检验中心要持续组织开展室间质评工作,并做好相关技术指导和支持。国家卫生健康委临床检验中心已将《全国新型冠状病毒核酸检测室间质量评价结果报告》发送至各省级临床检验中心,请相关医疗机构做好质量改进工作。
五、加强实验室生物安全管理,做好剩余样本处理
各地开展新冠病毒检测应当符合《病原微生物实验室生物安全管理条例》(国务院令第424号)有关规定,并执行《新型冠状病毒实验室生物安全指南(第二版)》(国卫办科教函〔2020〕70号)要求,切实加强生物安全管理。各省级卫生健康行政部门要结合实际情况研究提出本区域实验室剩余生物样本处置意见,医疗机构和疾控机构要落实主体责任,做好样本的使用、保存与销毁等工作。
国务院应对新型冠状病毒肺炎疫情联防原由网联控机制综合组
(代章)
2020年4月18日
科技部:批准建设国家人类疾病动物模型资源库
15日,科技部网站公布《科技部财政部关于批准建设国家人类疾病动物模型资源库的通知》。为进一步推动人类疾病动物模型资源利用和开放共享,依据《国家科技资源共享服务平台管理办法》,科技部、财政部决定批准建设国家人类疾病动物模型资源库,纳入国家科技资源共享服务平台管理。
据悉,国家人类疾病动物模型资源库依托单位是中国医学科学院实验动物研究所,主任为秦川,主管部门为卫生健康委。
该通知指出,请卫生健康委组织依托单位根据管理办法要求,制定五年建设运行实施方案,加强相关科技资源整合汇聚,强化研究开发与分析利用,推进开放共享,提升科技资源使用效率和科技创新支撑能力,完善科技资源存储、管理和安全所需基础设施,创新运行管理机制,加强评价考核组织管理,充分发挥法人单位主体责任,为科技创新和社会发展提供高质量的科技资源共享服务。
国家市场监督管理总局:口罩等防疫用品出口欧盟准入信息指南
一、CE标志制度
CE标志制度是欧盟对产品进入欧盟市场进行的监管方式。加贴CE标志的产品表明产品符合欧盟有关安全、健康、环保等法规要求,可以在欧盟27个成员国、欧洲贸易自由区的4个国家、以及英国和土耳其合法上市销售。按照欧盟规定,不同产品采用不同的评价方式加贴CE标志,主要有两种方式:绝大部分产品是制造商采取自我符合性声明方式,就可以加贴CE标志;部分风险相对更高的产品需要经过欧盟授权的第三方机构,即公告机构(Notified Body)进行符合性评定后,方可加贴CE标志。
欧盟针对不同的产品制定了不同的法规(指令),比如儿童玩具、低电压电器、个人防护器具、医疗器械等都有对应的法规(指令)。欧盟法规(指令)规定了对应产品的质量安全基本要求,以及上市的流程和合格评定程序。
产品经制造商自我声明加贴CE标志的流程:制造商必须确保自己的产品符合欧盟法规,产品是安全有效的,并建立相关技术文件,签署符合性声明,到成员国主管当局注册登记之后,即可在产品加贴CE标志进入欧盟销售。
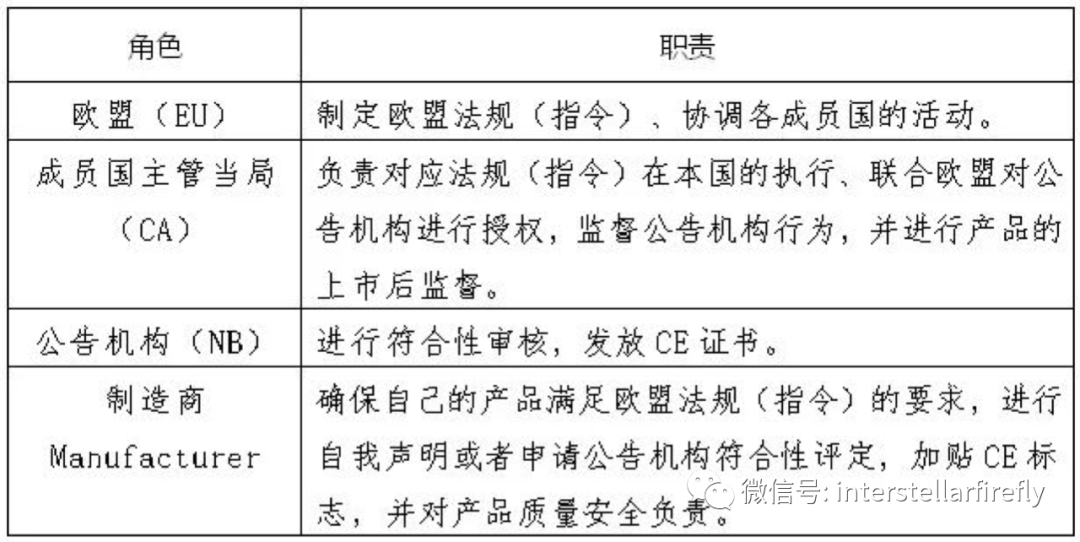
产品经公告机构符合性评定后加贴CE标志的流程:产品制造商向公告机构提出申请,公告机构为制造商提供符合性评定服务,制造商及产品符合法规要求的,向制造商发放CE证书。制造商依据CE证书签署符合性声明,产品加贴CE标志后就可以进入欧盟市场。下表列举了欧盟、成员国的主管当局、公告机构和制造商的职责。
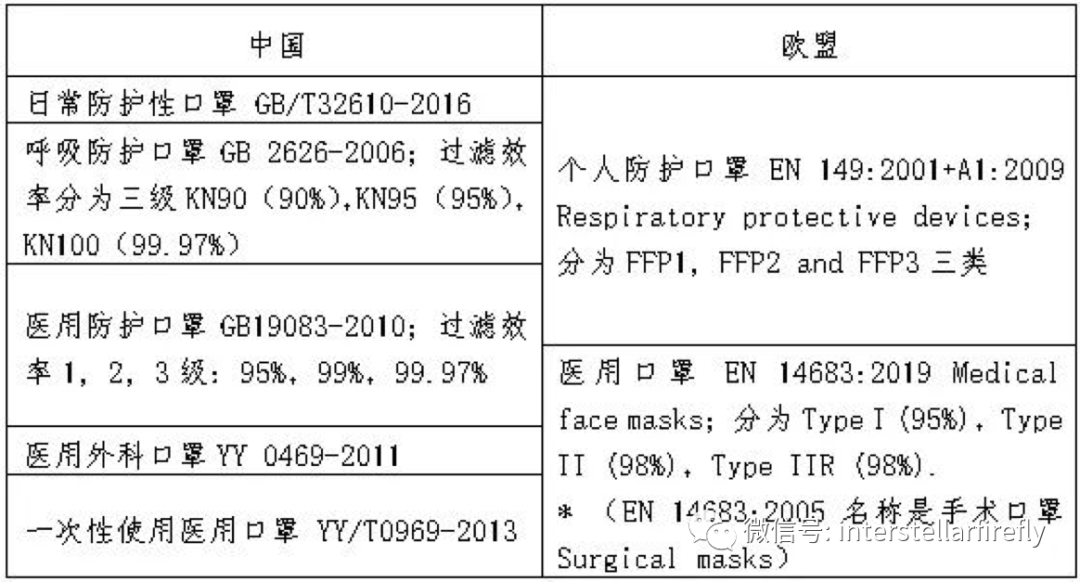
二、中欧口罩分类及相应标准
口罩在欧盟根据预期用途的不同,分为医用口罩和个人防护口罩两种,分别归属医疗器械条例EU2017/745(MDR)或医疗器械指令93/42/EEC(MDD)和个人防护设备条例EU2016/425(PPE)进行管理。如何判定具体产品属于哪一种口罩,需参照对应的法规规定和标准要求。
我国通常将口罩分为民用口罩和医用口罩。为便于理解,特将中国口罩类型及标准和欧盟的口罩类型及适用标准相对应,帮助大家了解您的口罩可能对应的是那种欧盟口罩,以及需要满足那个标准的要求。需要说明的是这种对应并不是严格的对应,并且中欧标准要求也有差异,请大家自己根据标准的详细要求分析并判定。
三、口罩出口欧盟的法规要求
(一)医用口罩
按照MDD或者MDR的要求,医用非灭菌口罩可以由制造商采取自我声明方式,加贴CE标志后上市销售。而医用灭菌口罩必须经公告机构符合性评定,才能加贴CE标志上市销售。但不管是否需要公告机构符合性评定,制造商都需要按照法规要求,参照相关标准或者满足欧盟质量要求的标准进行测试,以证实产品安全有效,并建立技术文件和质量管理体系,保证产品的质量安全和持续有效。
1.技术文件要求:
参照MDR法规附录II和附录III的要求(MDD为附录7),技术文件通常包括以下七个部分:
器械的描述和规范,包括名称、预期用途、分类、原料、构成、技术规范等。
产品的标签和(或)说明书
产品设计和制造的相关的信息
满足基本安全和通用性能的要求(附录I GSPR)
受益和风险分析,及风险管理文档
产品的验证和确认,包括临床前的测试和临床(评估)数据
上市后监督计划
2.制造商质量管理系要求:
质量管理体系可以参照协调性标准ISO 13485:2016进行。需要说明的是:质量管理体系需要参照ISO13485:2016来运行或者审核,但对于公告机构符合性评定来说,ISO13485认证证书并不是必须或者强制原由网的,但多数的制造商都会选择取得ISO 13485认证证书,这样可以提高客户对制造商能满足法规要求及产品质量保证的信心。
3.制造商授权欧盟代表
对于欧盟境外的制造商(如中国的制造商),需要在欧盟境内授权一个欧盟代表,代替制造商在欧盟进行相关活动,比如在主管当局进行自我声明产品的登记和不良事件的报告等。制造商需要和授权欧盟代表签订协议,并规定各自承担的职责。按照新的MDR法规,制造商需要将整套的技术文件提交给欧盟代表,以便主管当局备查。
(二)个人防护口罩
按照PPE法规要求,个人防护口罩需要有公告机构审核发放的CE证书,才能在欧盟合法上市销售。根据PPE法规关于符合性的相关规定,制造商需要建立相应技术文件,并满足EN149:2001+A1:2009的规格和测试要求。和医用口罩相比,个人防护口罩至少需获得两张公告机构的证书,即按照附录五的型式检验证书,按照附录七(Module C2)的证书或者附录八(Module D)的证书,详见下图:
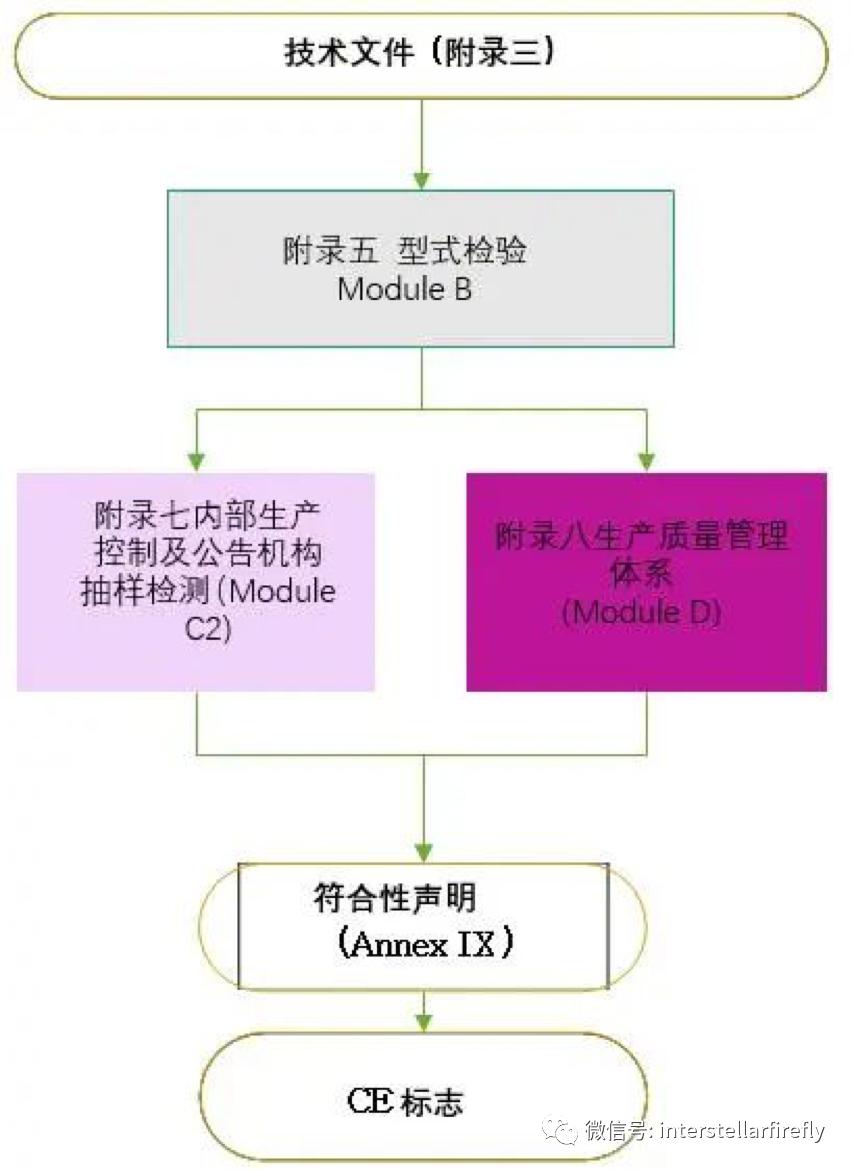
为了便于大家更清楚的了解医用口罩和个人防护口罩出口欧盟的流程异同,特归纳成下表,供大家参考。
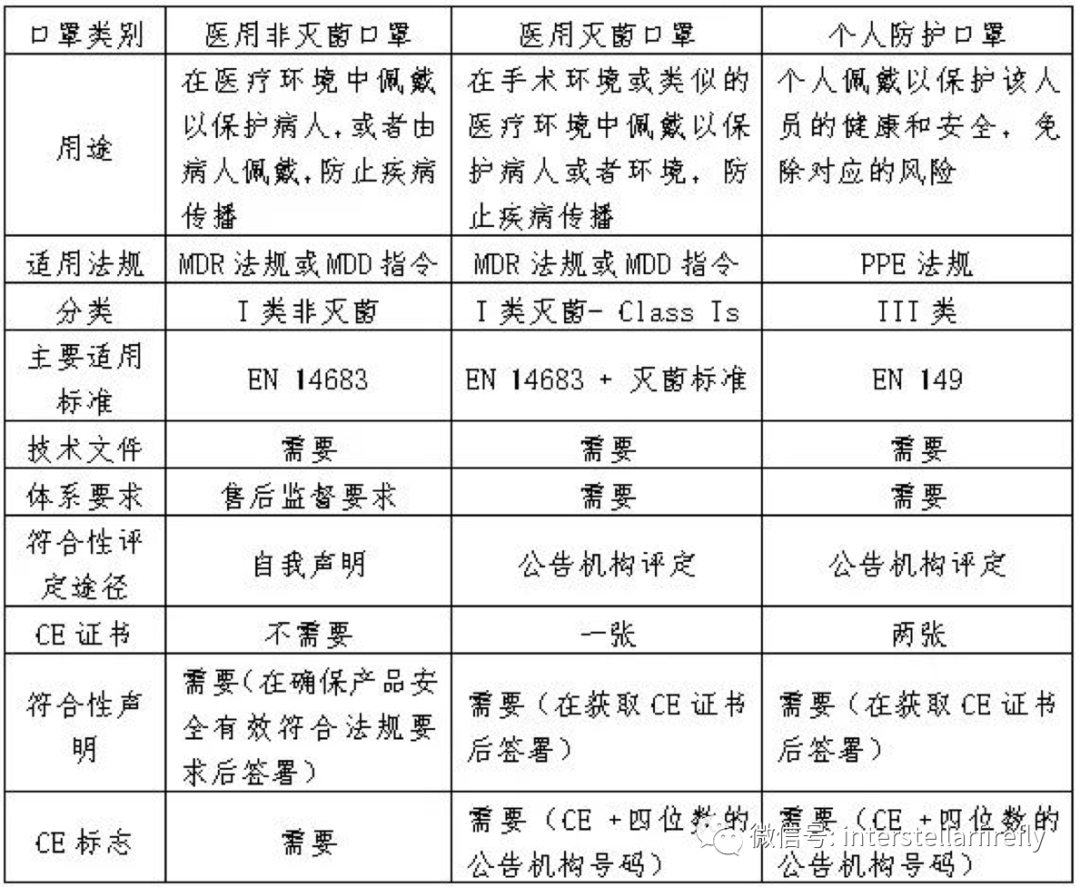
国家药监局:2020年3月批准注册医疗器械产品目录
2020年3月,国家药品监督管理局共批准注册医疗器械产品172个。其中,境内第三类医疗器械产品131个,进口第三类医疗器械产品18个,进口第二类医疗器械产品22个,港澳台医疗器械产品1个(具体产品见附件)。
序号 |
产品名称 |
注册人名称 |
注册证编号 |
境内第三类医疗器械 |
|||
1 |
新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
迈克生物股份有限公司 |
国械注准20203400184 |
2 |
化疗注药泵 |
爱普科学仪器(江苏)有限公司 |
国械注准20203140192 |
3 |
癌抗原125检测试剂盒(化学发光法) |
上海复星长征医学科学有限公司 |
国械注准20203400193 |
4 |
乙型肝炎病毒e抗体测定试剂盒(化学发光微粒子免疫检测法) |
厦门万泰凯瑞生物技术有限公司 |
国械注准20203400194 |
5 |
总前列腺特异抗原检测试剂盒(化学发光法) |
上海复星长征医学科学有限公司 |
国械注准20203400195 |
6 |
CYP2C19基因多态性检测试剂盒(荧光PCR熔解曲线法) |
踏石生物科技(苏州)有限公司 |
国械注准20203400196 |
7 |
生物可吸收冠脉雷帕霉素洗脱支架系统 |
山东华安生物科技有限公司 |
国械注准20203130197 |
8 |
新型冠状病毒(2019-nCoV)抗体检测试剂盒(磁微粒化学发光法) |
厦门万泰凯瑞生物技术有限公司 |
国械注准20203400198 |
9 |
新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(胶体金法) |
广东和信健康科技有限公司 |
国械注准20203400199 |
10 |
铁蛋白检测试剂盒(化学发光法) |
上海复星长征医学科学有限公司 |
国械注准20203400200 |
11 |
多肿瘤标志物质控品 |
上海透景诊断科技有限公司 |
国械注准20203400201 |
12 |
人附睾蛋白4检测试剂盒(化学发光法) |
上海复星长征医学科学有限公司 |
国械注准20203400202 |
13 |
细胞角蛋白19片段检测试剂盒(化学发光法) |
上海复星长征医学科学有限公司 |
国械注准20203400203 |
14 |
游离前列腺特异抗原检测试剂盒(化学发光法) |
上海复星长征医学科学有限公司 |
国械注准20203400204 |
15 |
糖类抗原72-4测定试剂盒(化学发光免疫分析法) |
上海透景诊断科技有限公司 |
国械注准20203400205 |
16 |
肿瘤相关抗原242测定试剂盒(化学发光免疫分析法) |
上海透景诊断科技有限公司 |
国械注准20203400206 |
17 |
癌胚抗原检测试剂盒(化学发光法) |
上海复星长征医学科学有限公司 |
国械注准20203400207 |
18 |
葡萄糖-6-磷酸脱氢酶基因检测试剂盒(PCR+导流杂交法) |
潮州凯普生物化学有限公司 |
国械注准20203400208 |
19 |
神经元特异性烯醇化酶检测试剂盒(化学发光法) |
上海复星长征医学科学有限公司 |
国械注准20203400209 |
20 |
丁丙诺啡检测试剂盒(胶体金法) |
杭州奥泰生物技术股份有限公司 |
国械注准20203400210 |
21 |
糖类抗原50测定试剂盒 (化学发光免疫分析法) |
上海透景诊断科技有限公司 |
国械注准20203400211 |
22 |
新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
武汉明德生物科技股份有限公司 |
国械注准20203400212 |
23 |
金属髓内针 |
苏州优贝特医疗器械有限公司 |
国械注准20203130213 |
24 |
金属髓内针 |
四川阿尔泰医疗器械有限公司 |
国械注准20203130214 |
25 |
圈套器套装 |
威海维心医疗设备有限公司 |
国械注准20203030215 |
26 |
胶原蛋白海绵 |
天津世纪康泰生物医学工程有限公司 |
国械注准20203140216 |
27 |
PTCA球囊导管 |
湖南埃普特医疗器械有限公司 |
国械注准20203030217 |
28 |
椎间融合器 |
重庆富沃思医疗器械有限公司 |
国械注准20203130218 |
29 |
金属锁定接骨螺钉 |
重庆富沃思医疗器械有限公司 |
国械注准20203130219 |
30 |
硬脑(脊)膜补片 |
天新福(北京)医疗器材股份有限公司 |
国械注准20203130220 |
31 |
颈椎前路固定系统 |
重庆富沃思医疗器械有限公司 |
国械注准20203130221 |
32 |
一次性使用精密过滤输液器 带针 |
江西科伦医疗器械制造有限公司 |
国械注准20203140222 |
33 |
微导丝 |
湖南瑞康通科技发展有限公司 |
国械注准20203030223 |
34 |
血管内通路导管系统 |
威海禾木吉瑞生物科技有限公司 |
国械注准20203030224 |
35 |
CD3/CD16+CD56/CD45/CD4/CD19/CD8检测试剂盒(流式细胞仪法) |
艾森生物(杭州)有限公司 |
国械注准20203400225 |
36 |
细胞角蛋白19片段检测试剂盒(化学发光免疫分析法) |
基蛋生物科技股份有限公司 |
国械注准20203400226 |
37 |
腺病毒IgM抗体检测试剂盒(磁微粒化学发光法) |
郑州安图生物工程股份有限公司 |
国械注准20203400227 |
38 |
葡萄糖6-磷酸脱氢酶(G6PD)检测试剂盒(比值法) |
广州市米基医疗器械有限公司 |
国械注准20203400228 |
39 |
二亚甲基双氧安非他明检测试剂盒(胶体金法) |
杭州奥泰生物技术股份有限公司 |
国械注准20203400229 |
40 |
CD3/CD16+CD56/CD45/CD19检测试剂盒(流式细胞仪法) |
艾森生物(杭州)有限公司 |
国械注准20203400230 |
41 |
糖类抗原19-9检测试剂盒(化学发光免疫分析法) |
基蛋生物科技股份有限公司 |
国械注准20203400231 |
42 |
糖类抗原50检测试剂盒(化学发光免疫分析法) |
基蛋生物科技股份有限公司 |
国械注准20203400232 |
43 |
癌抗原125检测试剂盒(化学发光免疫分析法) |
基蛋生物科技股份有限公司 |
国械注准20203400233 |
44 |
神经元特异性烯醇化酶检测试剂盒(化学发光免疫分析法) |
基蛋生物科技股份有限公司 |
国械注准20203400234 |
45 |
葡萄糖6-磷酸脱氢酶(G6PD)检测试剂盒(比值法) |
广州市米基医疗器械有限公司 |
国械注准20203400235 |
46 |
丙型肝炎病毒抗体检测试剂盒(化学发光免疫分析法) |
苏州立禾生物医学工程有限公司 |
国械注准20203400236 |
47 |
梅毒螺旋体抗体检测试剂盒(化学发光免疫分析法) |
苏州立禾生物医学工程有限公司 |
国械注准20203400237 |
48 |
癌抗原15-3检测试剂盒(化学发光免疫分析法) |
基蛋生物科技股份有限公司 |
国械注准20203400238 |
49 |
新型冠状病毒(2019-nCoV)IgM/IgG抗体检测试剂盒(胶体金法) |
南京诺唯赞医疗科技有限公司 |
国械注准20203400239 |
50 |
新型冠状病毒(2019-nCoV)IgM/IgG抗体检测试剂盒(胶体金法) |
珠海丽珠试剂股份有限公司 |
国械注准20203400240 |
51 |
新型冠状病毒2019-nCoV核酸检测试剂盒(恒温扩增-实时荧光法) |
杭州优思达生物技术有限公司 |
国械注准20203400241 |
52 |
麻醉深度监测仪 |
浙江一洋医疗科技有限公司 |
国械注准20203070242 |
53 |
无创呼吸机 |
南京舒普思达医疗设备有限公司 |
国械注准20203080243 |
54 |
神经外科手术导航定位系统 |
北京柏惠维康科技有限公司 |
国械注准20203010244 |
55 |
半导体激光治疗仪 |
北京拓殖智业科技有限公司 |
国械注准20203090245 |
56 |
一次性使用固定弯标测导管 |
科塞尔医疗科技(苏州)有限公司 |
国械注准20203070246 |
57 |
手术刨削器 |
杭州好克光电仪器有限公司 |
国械注准20203010247 |
58 |
X射线计算机体层摄影设备 |
上海联影医疗科技有限公司 |
国械注准20203060248 |
59 |
乙型肝炎病毒表面抗体测定试剂盒(化学发光免疫分析法) |
苏州立禾生物医学工程有限公司 |
国械注准20203400249 |
60 |
乙型肝炎病毒表面抗原测定试剂盒(化学发光免疫分析法) |
苏州立禾生物医学工程有限公司 |
国械注准20203400250 |
61 |
乙型肝炎病毒核心抗体测定试剂盒(化学发光免疫分析法) |
苏州立禾生物医学工程有限公司 |
国械注准20203400251 |
62 |
乙型肝炎病毒e抗体测定试剂盒(化学发光免疫分析法) |
苏州立禾生物医学工程有限公司 |
国械注准20203400252 |
63 |
HER-2/neu蛋白测定试剂盒(化学发光免疫分析法) |
苏州立禾生物医学工程有限公司 |
国械注准20203400253 |
64 |
癌胚抗原(CEA)测定试剂盒(电化学发光免疫分析法) |
北京联众泰克科技有限公司 |
国械注准20203400254 |
65 |
癌抗原CA72-4(CA72-4)测定试剂盒(电化学发光免疫分析法) |
北京联众泰克科技有限公司 |
国械注准20203400255 |
66 |
戊型肝炎病毒IgG抗体测定试剂盒(化学发光免疫分析法) |
苏州立禾生物医学工程有限公司 |
国械注准20203400256 |
67 |
甲胎蛋白(AFP)测定试剂盒(电化学发光免疫分析法) |
北京联众泰克科技有限公司 |
国械注准20203400257 |
68 |
癌抗原CA15-3(CA15-3)测定试剂盒(电化学发光免疫分析法) |
北京联众泰克科技有限公司 |
国械注准20203400258 |
69 |
糖类抗原CA19-9(CA19-9)测定试剂盒(电化学发光免疫分析法) |
北京联众泰克科技有限公司 |
国械注准20203400259 |
70 |
戊型肝炎病毒IgM抗体测定试剂盒(化学发光免疫分析法) |
苏州立禾生物医学工程有限公司 |
国械注准20203400260 |
71 |
乙型肝炎病毒e抗原测定试剂盒(化学发光免疫分析法) |
苏州立禾生物医学工程有限公司 |
国械注准20203400261 |
72 |
癌抗原CA125(CA125)测定试剂盒(电化学发光免疫分析法) |
北京联众泰克科技有限公司 |
国械注准20203400262 |
73 |
人工膝关节假体 |
常州鼎健医疗器械有限公司 |
国械注准20203130263 |
74 |
解剖型金属接骨板 |
西藏寰驰医疗器械有限公司 |
国械注准20203130264 |
75 |
锁定接骨板钉系统 |
西藏寰驰医疗器械有限公司 |
国械注准20203130265 |
76 |
直型金属接骨板(非锁定) |
西藏寰驰医疗器械有限公司 |
国械注准20203130266 |
77 |
一次性使用输液器 带针 |
江苏治宇医疗器材有限公司 |
国械注准20203140267 |
78 |
椎间融合器 |
江苏国立医疗器械有限公司 |
国械注准20203130268 |
79 |
聚羧酸锌水门汀 |
河南省民健齿科材料有限公司 |
国械注准20203170269 |
80 |
带袢钛板-组件 |
运怡(北京)医疗器械有限公司 |
国械注准20203130270 |
81 |
空心接骨螺钉(非锁定) |
厦门德朗格医疗科技有限公司 |
国械注准20203130271 |
82 |
金属交锁髓内钉 |
焦作市新港医疗设备有限公司 |
国械注准20203130272 |
83 |
一次性使用输液器 带针 |
山东朱氏药业集团有限公司 |
国械注准20203140273 |
84 |
一次性使用避光输液器 带针 |
山东朱氏药业集团有限公司 |
国械注准20203140274 |
85 |
远端塞 |
经纬医疗器材制造(深圳)有限公司 |
国械注准20203130275 |
86 |
中置器 |
经纬医疗器材制造(深圳)有限公司 |
国械注准20203130276 |
87 |
一次性使用输液器 带针 |
莲花医疗用品有限公司 |
国械注准20203140277 |
88 |
空心螺钉 |
纳通生物科技(北京)有限公司 |
国械注准20203130278 |
89 |
髋关节假体-股骨柄 |
经纬医疗器材制造(深圳)有限公司 |
国械注准20203130279 |
90 |
肋骨接骨板系统 |
上海凯利泰医疗科技股份有限公司 |
国械注准20203130280 |
91 |
牙科粘接剂 |
吉林省登泰克牙科材料有限公司 |
国械注准20203170281 |
92 |
椎板固定板系统 |
深圳市沃尔德外科医疗器械技术有限公司 |
国械注准20203130282 |
93 |
血液透析器 |
河南省驼人医疗科技有限公司 |
国械注准20203100283 |
94 |
牙胶尖 |
山东达雅鼎医疗器械有限公司 |
国械注准20203170284 |
95 |
脊柱内固定器-钉板系统 |
浙江康飞思医疗科技有限公司 |
国械注准20203130285 |
96 |
肋骨接骨板 |
重庆富沃思医疗器械有限公司 |
国械注准20203130286 |
97 |
一次性输液消毒接头 |
湖南三瑞生物科技有限责任公司 |
国械注准20203140287 |
98 |
非骨水泥髋臼系统 |
施乐辉外科植入物(北京)有限公司 |
国械注准20203130288 |
99 |
交锁髓内钉系统 |
浙江德康医疗器械有限公司 |
国械注准20203130289 |
100 |
金属骨针 |
重庆富沃思医疗器械有限公司 |
国械注准20203130290 |
101 |
分隔膜无针接头 |
北京天地和协科技有限公司 |
国械注准20203140291 |
102 |
一次性使用精密过滤输液器 带针 |
山东中保康医疗器具有限公司 |
国械注准20203140292 |
103 |
一次性使用精密过滤输液器 带针 |
山东中保康医疗器具有限公司 |
国械注准20203140293 |
104 |
一次性使用输液器 带针 |
山东中保康医疗器具有限公司 |
国械注准20203140294 |
105 |
注射用修饰透明质酸钠凝胶 |
华熙生物科技股份有限公司 |
国械注准20203130295 |
106 |
一次性使用密闭式防针刺静脉留置针 |
河南慧超医疗器械有限公司 |
国械注准2原由网0203140296 |
107 |
可折叠人工晶状体 |
天津世纪康泰生物医学工程有限公司 |
国械注准20203160297 |
108 |
新型冠状病毒2019-nCoV核酸检测试剂盒(杂交捕获免疫荧光法) |
安邦(厦门)生物科技有限公司 |
国械注准20203400298 |
109 |
新型冠状病毒(2019-nCoV)核酸检测试剂盒(荧光PCR法) |
上海复星长征医学科学有限公司 |
国械注准20203400299 |
110 |
新型冠状病毒2019-nCoV核酸检测试剂盒(RNA捕获探针法) |
上海仁度生物科技有限公司 |
国械注准20203400300 |
111 |
新型冠状病毒2019-nCoV核酸检测试剂盒(RNA恒温扩增-金探针层析法) |
武汉中帜生物科技股份有限公司 |
国械注准20203400301 |
112 |
新型冠状病毒2019-nCoV核酸检测试剂盒(双扩增法) |
武汉中帜生物科技股份有限公司 |
国械注准20203400302 |
113 |
金属3D打印骨盆缺损匹配假体 |
北京爱康宜诚医疗器材有限公司 |
国械注准20203130303 |
114 |
金属骨针 |
常州华森医疗器械有限公司 |
国械注准20203130304 |
115 |
覆膜胆道支架套装 |
南京微创医学科技股份有限公司 |
国械注准20203130305 |
116 |
钛及钛合金人工牙种植体系统 |
西安康拓医疗技术有限公司 |
国械注准20203170306 |
117 |
一次性使用精密过滤输液器 带针 |
长春金康源医用器具有限公司 |
国械注准20203140307 |
118 |
双弯导丝 |
北京华脉泰科医疗器械有限公司 |
国械注准20203030308 |
119 |
一次性使用麻醉导管及接头 |
南昌贝欧特医疗科技股份有限公司 |
国械注准20203140309 |
120 |
一次性使用精密过滤输液器 带针 |
南阳市久康医疗器械有限公司 |
国械注准20203140310 |
121 |
一次性使用输液器 带针 |
南阳市久康医疗器械有限公司 |
国械注准20203140311 |
122 |
一次性使用延长管 |
湖南平安医械科技有限公司 |
国械注准20203140312 |
123 |
脊柱内固定系统 |
北京爱康宜诚医疗器材有限公司 |
国械注准20203130313 |
124 |
注射用交联透明质酸钠凝胶 |
上海其胜生物制剂有限公司 |
国械注准20203130314 |
125 |
一次性使用造影导管 |
安吉特(天津)科技有限公司 |
国械注准20203030315 |
126 |
一次性使用输液器 带针 |
山东中保康医疗器具有限公司 |
国械注准20203140316 |
127 |
椎板固定板系统 |
江苏百易得医疗科技有限公司 |
国械注准20203130317 |
128 |
微导管 |
湖南瑞康通科技发展有限公司 |
国械注准20203030318 |
129 |
冠状动脉球囊扩张导管 |
深圳市业聚实业有限公司 |
国械注准20203030319 |
130 |
可吸收性外科缝线 |
南京普立蒙医疗科技有限公司 |
国械注准20203020320 |
131 |
闭合夹 |
华融科创生物科技(天津)有限公司 |
国械注准20203020321 |
进口第三类医疗器械 |
|||
132 |
电子鼻咽喉内窥镜 |
XION GmbH |
国械注进20203060100 |
133 |
桩核树脂水门汀 |
META BIOMED CO., LTD. |
国械注进20203170104 |
134 |
热熔断三维弹簧圈 |
MicroVention, Inc. |
国械注进20203130105 |
135 |
人工牙种植体 |
Institut Straumann AG |
国械注进20203170106 |
136 |
颈椎前路椎间融合器 |
Medtronic Sofamor Danek USA, Inc. |
国械注进20203130123 |
137 |
带袢固定板系统 |
Biomet Sports Medicine |
国械注进20203130124 |
138 |
纵裂式外导引导管 |
St. Jude Medical Cardiac Rhythm Management Division |
国械注进20203030125 |
139 |
纵裂式内导管 |
St. Jude Medical Cardiac Rhythm Management Division |
国械注进20203030126 |
140 |
带亲水涂层的导管鞘组 |
Merit Medical Systems, Inc. |
国械注进20203030127 |
141 |
微导管 |
株式会社パイオラックスメディカルデバイス |
国械注进20203030128 |
142 |
髋臼系统 |
Smith & Nephew, Inc. |
国械注进20203130129 |
143 |
初次及翻修膝关节组件 |
DePuy (Ireland) |
国械注进20203130130 |
144 |
青光眼引流管 |
Allergan |
国械注进20203160132 |
145 |
单髁膝关节系统 |
MAKO SURGICAL CORP. |
国械注进20203130133 |
146 |
基台及配件 |
MegaGen Implant Co.,Ltd. |
国械注进20203170134 |
147 |
卵裂胚培养液 |
Vitrolife Sweden AB |
国械注进20203180135 |
148 |
导丝 |
Vascular Solutions LLC |
国械注进20203030136 |
149 |
椎间融合器 |
Medtronic Sofamor Danek USA, Inc. |
国械注进20203130137 |
进口第二类医疗器械 |
|||
150 |
一次性眼科手术用刀 |
SIDAPHARM P.C. |
国械注进20202160096 |
151 |
咽部神经肌肉刺激器 |
DJO, LLC |
国械注进20202090099 |
152 |
关节内窥镜手术器械 |
Biomet Sports Medicine |
国械注进20202040101 |
153 |
种植体附件取出用牙钻 |
OSSTEM IMPLANT Co., Ltd. |
国械注进20202170102 |
154 |
预处理剂 |
Kulzer GmbH |
国械注进20202170103 |
155 |
刺柏t6过敏原特异性IgE抗体检测试剂盒(荧光免疫法) |
Phadia AB |
国械注进20202400107 |
156 |
葎草w22特异性IgE抗体检测试剂盒(荧光免疫法) |
Phadia AB |
国械注进20202400108 |
157 |
抗2糖蛋白1结构域1IgG抗体质控品 |
INOVA Diagnostics, Inc. |
国械注进20202400109 |
158 |
梯牧草g6过敏原特异性IgE抗体检测试剂盒(荧光免疫法) |
Phadia AB |
国械注进20202400110 |
159 |
百幕达草g2过敏原特异性IgE抗体检测试剂盒(荧光原由网免疫法) |
Phadia AB |
国械注进20202400111 |
160 |
枫叶梧桐,伦敦悬铃木t11特异性IgE抗体检测试剂盒(荧光免疫法) |
Phadia AB |
国械注进20202400112 |
161 |
射线束扫描系统 |
Sun Nuclear Corporation |
国械注进20202050113 |
162 |
牙科电动马达系统 |
Kaltenbach & Voigt GmbH |
国械注进20202170114 |
163 |
医用电动诊疗床 |
Lojer Oy |
国械注进20202150115 |
164 |
医学图像处理软件 |
Siemens Healthcare GmbH |
国械注进20202210116 |
165 |
射线束扫描系统 |
Sun Nuclear Corporation |
国械注进20202050117 |
166 |
全自动免疫印迹仪 |
HUMAN Gesellschaft fur Biochemica und Diagnostica mbH |
国械注进20202220118 |
167 |
一次性使用无菌根管冲洗头 |
VDW GmbH |
国械注进20202170119 |
168 |
一次性使用间歇性导尿管 |
B. Braun Medical SAS |
国械注进20202140120 |
169 |
全瓷乳牙预成冠 |
NuSmile.Ltd |
国械注进20202170121 |
170 |
氧化锆瓷块 |
Genoss Co., Ltd. |
国械注进20202170122 |
171 |
牙科临时树脂水门汀 |
B.J.M.LABORATORIES LTD. |
国械注进20202170131 |
港澳台医疗器械 |
|||
172 |
医用辅助袜 |
杉蒲企業股份有限公司 |
国械注许20202090006 |
哈哈
The second story
白
1
报告
《 核酸检测行业创新报告》
哈哈
The third story
白
1
Lone Operator
——How to Survive & Thrive in the Modern Age
独行侠
——现代社会的生存与发展

他是一个完美的专业人士,有一种“能干”的态度,激励自己和他人尽力而为。
《Lone Operator》是现代斯巴达人的真实故事。Joseph N Teti至始至终保持谦虚,克服了贫穷、悲惨的损失和致残恐惧症,在三个特种作战部队中服役。作为被广泛认为是世界上最秘密的政府反恐部门的一员,他屡次冒着风险在阿富汗和伊拉克的残酷战斗中幸存下来。在特种作战中担任“尖兵”期间,他学到了推动他后来商业生涯的技能。
作为一个名经验丰富的企业家,他分享了在当今混乱和疯狂的世界中生存所需的关键技能,同时也分享了茁壮成长所需的关键技能。
在探索频道的热门节目《双重生存 Dual Survity》中,这位前联合主角在这个星球上最恶劣的环境中度过了难关,从斯里兰卡的丛林到阿曼的沙漠,再到挪威的冰川。他被认为是荒野和城市生存的双重专家,曾登上多家杂志的封面。
他的人生故事的核心就是克服一切困难,不惜一切代价赢得胜利,不断提高标准,让每一天都变得更好。
作者:Joseph N Teti
出版:2020.4.20
哈哈
The fourth story
白
1
猜猜看
- 问题
儿童早睡和肥胖有什么关系?

《PLOS ONE》:加州大学戴维斯分校的气溶胶科学家认为,无症状但感染了冠状病毒的人正常讲话可能产生足够的气溶胶粒子来传播感染——普通的说话会产生大量的呼吸颗粒的气溶胶,说话声音越大,释放出的粒子越多。有些"超级排放者",释放出的粒子是其他人的10倍。
问题请见上期文章: 创新智库 l “智能马桶“能让人们在如厕时就完成体检-第165期