【要点解读】
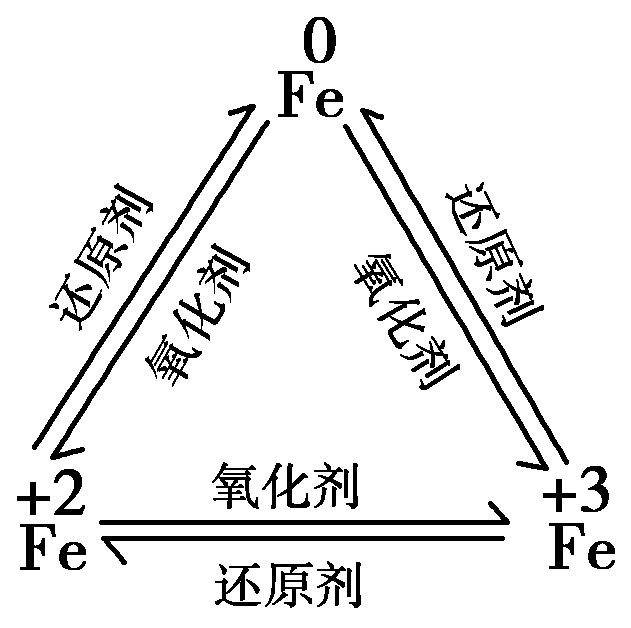
1.Fe只具有还原性,可以被氧化剂氧化
(1)与弱氧化剂反应
Fe能被S、Fe3+、Cu2+、H+等较弱氧化剂氧化为Fe2+,如:Fe+SFeS,Fe+2Fe3+=3Fe2+。
(2)与强氧化剂反应
Fe能被Cl2、HNO 3等强氧化剂氧化为Fe 3+,如:2Fe+3Cl 22FeCl3。
2.Fe2+既具有氧化性又具原由网有还原性
(1)与氧化剂反应
当Fe2+遇到强氧化剂(如Cl2、HNO3、KMnO4)时,被氧化为Fe3+,如:2Fe2++Cl2=2Fe3++2Cl-
(2)与还原剂反应
当Fe 2+遇到C、Al、Zn、CO等还原剂时,可以被还原为Fe,如:Fe 2++Zn=Zn 2++Fe,FeO+CO Fe+CO2
3.Fe3+具有较强氧化性,可被还原为Fe2+或Fe
(1)Fe3+被C、CO、Al等还原为Fe,如
Fe2O3+3CO 2Fe+3CO2,
Fe2O3+2Al //www.58yuanyou.com2Fe+Al 2O3
(2)Fe3+被Fe、Cu、I-等还原为Fe2+,如
2Fe3++Cu=www.58yuanyou.com2Fe 2++Cu 2+
【温馨提示】
(1)不同价态的铁及铁的化合物在相互转化时,注意所用氧化剂和还原剂的强弱不同。
(2)亚铁盐保存时,为了防止被氧化为铁盐,通常在溶液irVnqYGLzA中加少量还原铁粉或铁钉。
【名师点睛】酸性条件下硝酸根离子具有强氧化性,能将亚铁离子氧化为三价,二价铁浅绿色,三价铁为棕黄色
【重难点点睛】铁及其化合物推断突破口
(1)特征颜色及变化:
①Fe2+溶液:浅绿色;Fe 3+溶液:棕黄色;Fe(OH) 3胶体:红褐色;Fe(OH) 3:红褐色;Fe 2O原由网3:红棕色;FeO和Fe 3O4:黑色;
②Fe2+溶液中加NaOH溶液:白色沉淀→灰绿色→红褐色;
③Fe3+溶液中加KSCN溶液变红色。
(2)特征价态变化:
铁为常见的变价金属。